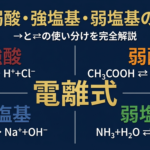
【前回の記事】強酸・弱酸・強塩基・弱塩基の電離式
まだ練習問題を解いていない方はこちらから先に挑戦しましょう!
▶ 前回の記事(練習問題)を見る
前回の練習問題5問、解けましたか?この記事では全5問の解答と解説を丁寧に説明します。電離式は入試で頻出なので、書き方をしっかり確認しましょう!
📋 解答一覧(まず答え合わせ)
- 問題1:①HNO₃→H⁺+NO₃⁻ ②CH₃COOH⇌H⁺+CH₃COO⁻ ③H₂SO₄→2H⁺+SO₄²⁻ ④H₂CO₃⇌H⁺+HCO₃⁻ ⑤HF⇌H⁺+F⁻
- 問題2:①NaOH→Na⁺+OH⁻ ②NH₃+H₂O⇌NH₄⁺+OH⁻ ③Ca(OH)₂→Ca²⁺+2OH⁻ ④Al(OH)₃⇌Al³⁺+3OH⁻ ⑤Ba(OH)₂→Ba²⁺+2OH⁻
- 問題3:①H₂S=弱酸(H₂S⇌H⁺+HS⁻) ②KOH=強塩基(KOH→K⁺+OH⁻) ③HCN=弱酸(HCN⇌H⁺+CN⁻) ④Mg(OH)₂=弱塩基(Mg(OH)₂⇌Mg²⁺+2OH⁻) ⑤HBr=強酸(HBr→H⁺+Br⁻)
- 問題4:第1段階:H₃PO₄⇌H⁺+H₂PO₄⁻ 第2段階:H₂PO₄⁻⇌H⁺+HPO₄²⁻ 第3段階:HPO₄²⁻⇌H⁺+PO₄³⁻
- 問題5:弱酸・弱塩基は電離と再結合が同時に起こり平衡状態(化学平衡)になるため⇌を使う
📝 この記事のまとめ
- 強酸・強塩基は→(完全電離)、弱酸・弱塩基は⇌(部分電離)
- HFだけは弱酸(HCl・HBr・HIは強酸):H-F結合が強いため
- NH₃の電離式は特殊:NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
- 多価の酸・塩基はH⁺・OH⁻を1個ずつ段階的に放出する
- Ca(OH)₂・Ba(OH)₂は強塩基、Mg(OH)₂は弱塩基
- ⇌を使う理由:電離と再結合が同時に起こる化学平衡のため

コメント