【前回の記事】酸化還元反応シリーズ まとめと演習 解答・解説
酸化還元反応シリーズの総復習をまだしていない方はこちらから!
▶ 前回の記事を読む
酸化還元反応シリーズお疲れ様でした!次のテーマは金属のイオン化傾向です。金属がどれだけ陽イオンになりやすいかを表すイオン化傾向は、酸化還元反応と深く結びついています。覚え方から具体的な反応例まで、丁寧に解説します!
- イオン化傾向とは何か
- イオン化傾向の順番と語呂合わせ
- イオン化傾向と反応性の関係
- 酸との反応・水との反応・酸化物の生成
- 不動態とは何か
- 練習問題10問
金属原子が電子を放出して陽イオンになりやすさを表したものをイオン化傾向といいます。イオン化傾向が大きい金属ほど酸化されやすく、反応性が高いです。
金属原子が電子を放出して陽イオンになる反応=酸化
主要な金属をイオン化傾向の大きい順に並べたものがイオン化列です。
← スクロールして全体を確認できます
「リッチに貸そうかな、まぁあてにすんな、ひどすぎる借金」
🔴 リッチに貸そうかな(イオン化傾向 大)
🟡 まぁあてにすんな
🟢 ひどすぎる借金(イオン化傾向 小)
🔴 イオン化傾向 大
- 電子を放出しやすい
- 陽イオンになりやすい
- 酸化されやすい・反応しやすい
🟢 イオン化傾向 小
- 電子を放出しにくい
- 単体のまま存在しやすい
- 酸化されにくい・反応しにくい
- Au・Ptなどが自然界に単体で産出される理由
イオン化傾向の大きさによって、水・酸・空気との反応性が異なります。
| 反応の種類 | 反応する金属 | 反応例 |
|---|---|---|
| 常温の水と反応 | Li・K・Ca・Na | 2Na + 2H₂O → 2NaOH + H₂ |
| 熱水・水蒸気と反応 | Mg(熱水)・Al・Zn・Fe(水蒸気) | Mg + 2H₂O → Mg(OH)₂ + H₂ 3Fe + 4H₂O → Fe₃O₄ + 4H₂ |
| 希酸と反応してH₂発生 | Li〜Pb(H₂より左) | Zn + H₂SO₄ → ZnSO₄ + H₂ |
| 酸化力のある酸と反応 | Cu・Hg・Ag(希硝酸・濃硝酸・熱濃硫酸) | 3Cu + 8HNO₃(希) → 3Cu(NO₃)₂ + 2NO + 4H₂O |
| 王水のみで反応 | Pt・Au | 濃塩酸と濃硝酸を3:1で混合した王水 |
イオン化列でH₂より左側の金属(Li〜Pb)は希硫酸や塩酸と反応して水素を発生します。
H₂より右の金属(Cu・Hg・Ag・Pt・Au)は希酸とは反応しません。
ただし酸化力のある酸(希硝酸・濃硝酸・熱濃硫酸)とは反応します(Pt・Auを除く)。
Naは常温の水と激しく反応し、水酸化ナトリウムと水素を発生します。
Naのイオン化:Na → Na⁺ + e⁻(酸化)
H₂Oの変化:2H₂O + 2e⁻ → H₂ + 2OH⁻(還元)
まず半反応式を書いてから化学反応式を作ります。
Znの酸化数:0 → +2(2増加)→ e⁻×2個(右辺へ)
Hの酸化数:+1 → 0(1減少)× 2個 → e⁻×2個(左辺へ)
ZnはH₂よりイオン化傾向が大きいため、H⁺から電子を奪ってH₂を発生させます。
CuはH₂よりイオン化傾向が小さく、希硫酸とは反応しません。しかし酸化力のある硝酸とは反応します。半反応式から作ります。
Nの酸化数:+5 → +2(3減少)→ e⁻×3個(左辺へ)
Cuの酸化数:0 → +2(2増加)→ e⁻×2個(右辺へ)
不動態とは、金属の表面に緻密な酸化物の膜が形成され、それ以上内部が侵食されなくなる状態のことです。
- Fe(鉄)・Al(アルミニウム)・Ni(ニッケル)が代表的
- 濃硝酸・濃硫酸に浸けると表面に酸化物の膜が形成される
- 一度不動態になると酸にも溶けなくなる
FeやAlは希硝酸とは反応しますが、濃硝酸では不動態になり反応しません。
入試では「Alは希塩酸に溶けるが、濃硝酸には溶けない」のように問われることが多いです。
イオン化傾向の大きい金属を、イオン化傾向の小さい金属のイオンを含む溶液に入れると、小さい方の金属が析出します。
Znのイオン化傾向 > Cuのイオン化傾向
→ ZnがCu²⁺に電子を渡す → Znが溶け出し、Cuが析出する
Zn:0 → +2(酸化) Cu²⁺:+2 → 0(還元)
Cuのイオン化傾向 > Agのイオン化傾向
→ CuがAg⁺に電子を渡す → Cuが溶け出し、Agが析出する
Cu:0 → +2(酸化) Ag⁺:+1 → 0(還元)
析出した金属が木の枝のような樹状の結晶として成長する現象を金属樹といいます。
🌳 銅樹(どうじゅ)
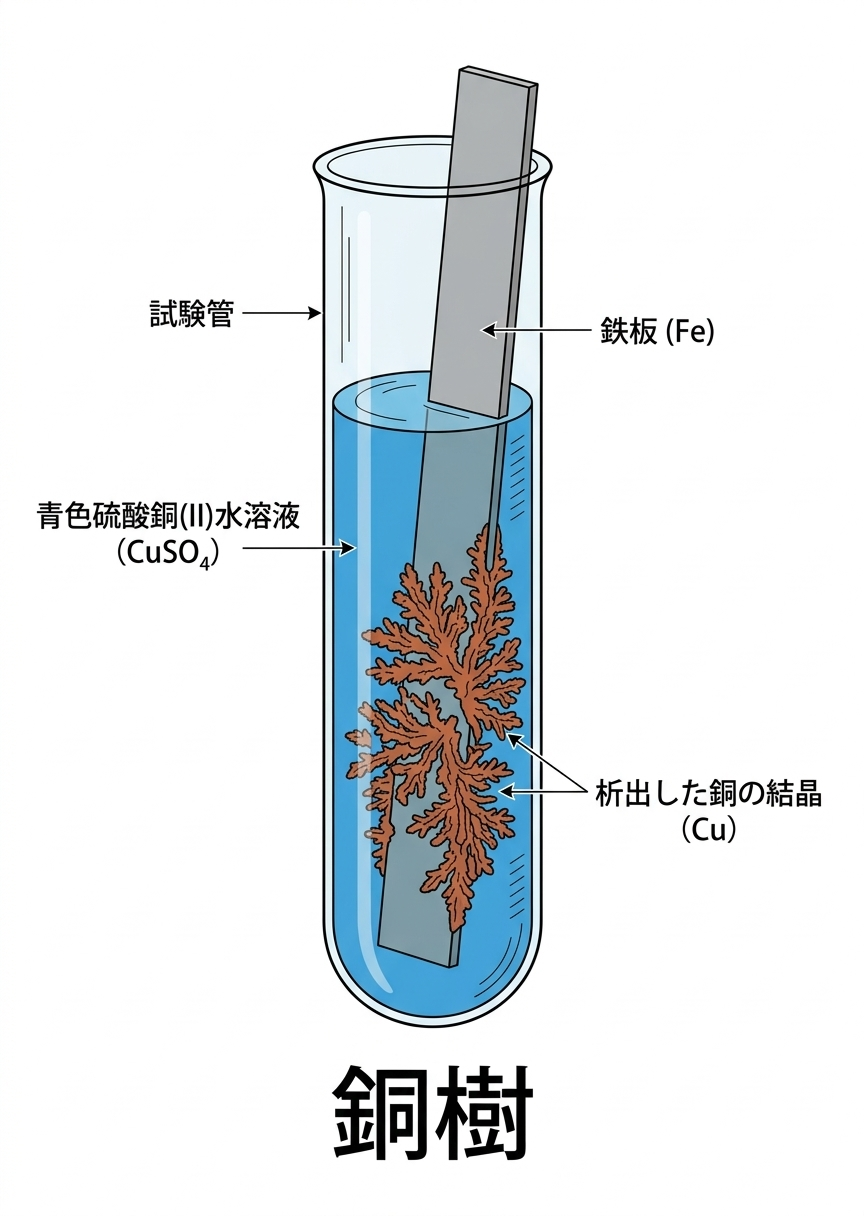
Fe(鉄)をCuSO₄水溶液に入れると、鉄の表面に赤みがかった銅の結晶が樹状に析出します。
Fe + CuSO₄ → FeSO₄ + Cu
※ ZnをCuSO₄に入れた場合も同様に銅樹が形成されます
🌳 銀樹(ぎんじゅ)
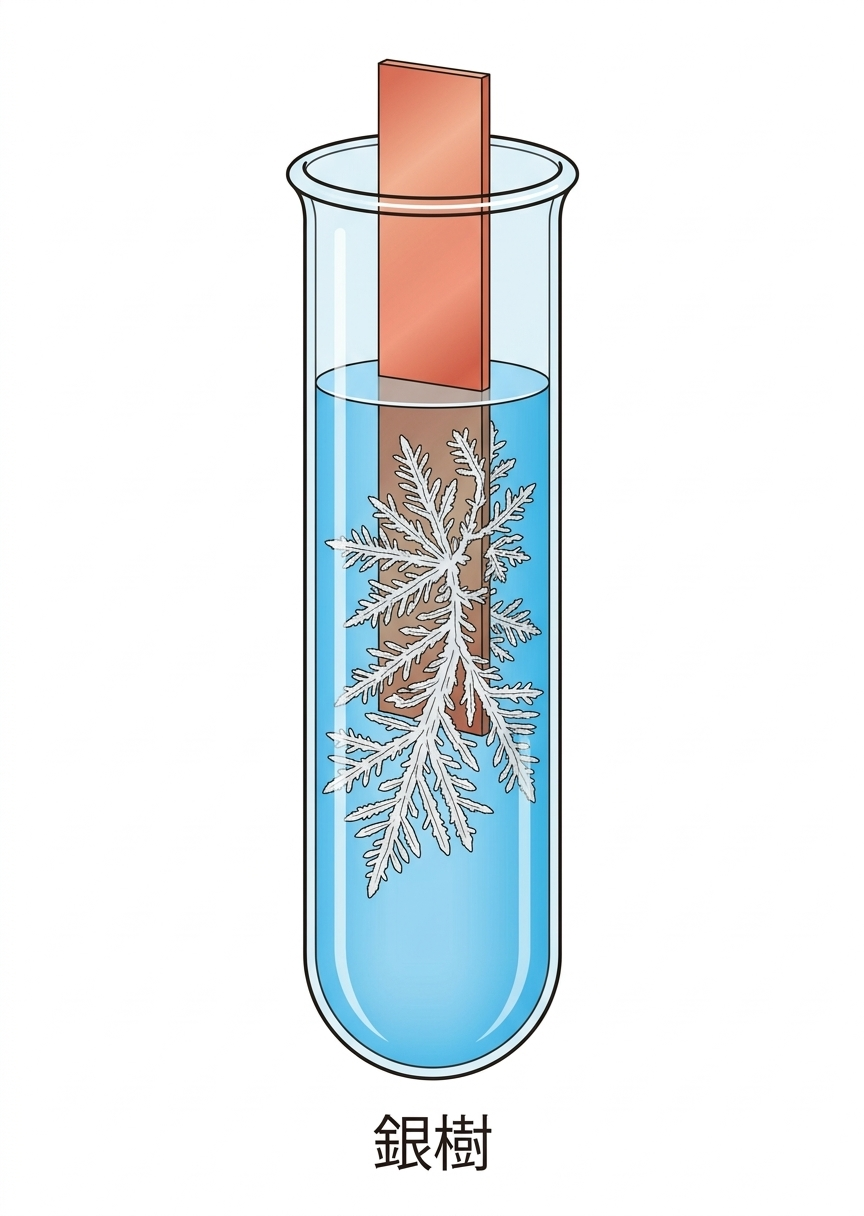
Cu(銅)をAgNO₃水溶液に入れると、銅の表面に白銀色の銀の結晶が樹状に析出します。
Cu + 2AgNO₃ → Cu(NO₃)₂ + 2Ag
※ 溶液は無色→青色(Cu²⁺の色)に変化します
- 析出した金属が枝分かれした結晶を形成する現象
- イオン化傾向の差が大きいほど反応が速く、樹状結晶が成長しやすい
- 銅樹:赤みがかった銅の結晶 銀樹:白銀色の銀の結晶
- 銀樹形成時は溶液が無色→青色に変化(Cu²⁺が溶け出すため)
- イオン化傾向:金属が陽イオンになりやすさの順番
- 語呂合わせ:「リッチに貸そうかな、まぁあてにすんな、ひどすぎる借金」(Li→K→Ca→Na→Mg→Al→Zn→Fe→Ni→Sn→Pb→H₂→Cu→Hg→Ag→Pt→Au)
- H₂より左の金属は希酸からH₂を発生させる
- Cu・Hg・Agは酸化力のある酸(硝酸・熱濃硫酸)とのみ反応する
- 不動態:Fe・Al・Niが濃硝酸・濃硫酸で形成する酸化膜
- イオン化傾向が大きい金属>小さい金属イオン → 小さい方が析出
✏️ 練習問題【全10問】
解答・解説は次の記事で確認しましょう!
次の金属をイオン化傾向の大きい順に並べよ。
Cu、Al、Na、Fe、Ag
次の金属のうち、常温の水と反応するものをすべて選べ。
Na、Mg、Fe、Ca、Cu、K
次の金属のうち、希塩酸と反応して水素を発生させるものをすべて選べ。
Zn、Cu、Al、Ag、Fe、Pb
鉄(Fe)を濃硝酸に入れたとき、どのような変化が起こるか説明せよ。
銅板をAgNO₃水溶液に入れたとき、何が起こるか。化学反応式を書いて説明せよ。
鉄板をCuSO₄水溶液に入れたときの化学反応式を書け。
亜鉛と希硝酸(HNO₃)の化学反応式を書け。
次のうち、Pt(白金)を溶かすことができるものを選べ。
①希塩酸 ②濃硝酸 ③王水 ④希硫酸
Mg、Zn、Feを希塩酸に入れたとき、水素の発生が最も激しいのはどれか。イオン化傾向をもとに理由も説明せよ。
硫酸銅(CuSO₄)水溶液にAl片を入れた。このとき起こる反応をイオン反応式で書け。また、Al片はどのように変化するか説明せよ。



コメント