【前回の記事】電池の仕組み③鉛蓄電池
鉛蓄電池の放電・充電の仕組みをまだ確認していない方はこちらから!
▶ 前回の記事を読む
ボルタ電池・ダニエル電池・鉛蓄電池の3つを学んできました。この記事では電池シリーズの総復習として練習問題に挑戦しましょう!解答・解説は次の記事で確認できます。
- 電池:イオン化傾向の差を利用して化学エネルギー→電気エネルギーに変換
- 負極:イオン化傾向が大きい→酸化・e⁻放出
- 正極:イオン化傾向が小さい→還元・e⁻受取
- ボルタ電池:Zn(負極)・Cu(正極)・希硫酸 → 分極が起こる
- ダニエル電池:Zn(ZnSO₄)・Cu(CuSO₄)・素焼き板 → 分極なし・安定
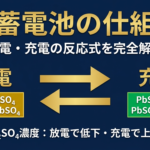
- 鉛蓄電池:Pb(負極)・PbO₂(正極)・希硫酸 → 二次電池・充電可能
わからない問題があったら復習しましょう!
▶ 電池①ボルタ電池の記事を読む
✏️ 問題1〜5
次の( )に適切な語句を入れよ。
ボルタ電池では、イオン化傾向の(ア)金属が負極になり、(イ)反応が起こる。イオン化傾向の(ウ)金属が正極になり、(エ)反応が起こる。
ボルタ電池について、次の問いに答えよ。
① 負極・正極の材料をそれぞれ答えよ。
② 電解液を答えよ。
③ 負極・正極それぞれの反応式を書け。
④ 全体の反応式を書け。
ボルタ電池で電流を流し続けると、電圧が急激に低下する。この現象を何というか。またその理由を説明せよ。
ボルタ電池において、電子の流れる方向と電流の流れる方向をそれぞれ答えよ。
ボルタ電池のZn板とCu板の代わりに、FeとCuを使った場合を考える。
① どちらが負極になるか。
② 負極・正極のそれぞれの反応式を書け。
③ Zn・Cuを使った場合とFe・Cuを使った場合で、起電力はどちらが大きいか理由も含めて答えよ。
わからない問題があったら復習しましょう!
▶ 電池②ダニエル電池の記事を読む
✏️ 問題6〜10
ダニエル電池について、次の問いに答えよ。
① 負極・正極の材料をそれぞれ答えよ。
② 負極側・正極側の電解液をそれぞれ答えよ。
③ 負極・正極それぞれの反応式を書け。
④ 全体の反応式を書け。
ダニエル電池で使われる素焼き板の役割を2つ答えよ。
ダニエル電池を長時間使用したとき、次のものはどのように変化するか答えよ。
① Zn板の質量 ② Cu板の質量 ③ CuSO₄水溶液の色
ボルタ電池とダニエル電池の最も大きな違いは何か。「分極」という語句を使って説明せよ。
ダニエル電池において、素焼き板を取り除いてZnSO₄とCuSO₄の2つの溶液を混合した場合、電池はどのような挙動を示すか。理由とともに説明せよ。
わからない問題があったら復習しましょう!
▶ 電池③鉛蓄電池の記事を読む
✏️ 問題11〜15
鉛蓄電池について、次の問いに答えよ。
① 負極・正極の材料をそれぞれ答えよ。
② 電解液を答えよ。
③ 放電時の負極・正極それぞれの反応式を書け。
④ 放電時の全体の反応式を書け。
鉛蓄電池の放電時と充電時について、次の問いに答えよ。
① 放電時にH₂SO₄の濃度はどうなるか。
② 充電時にH₂SO₄の濃度はどうなるか。
③ 充電時の全体の反応式を書け。
鉛蓄電池について、放電時のPbとPbO₂それぞれの酸化数の変化を答えよ。またそれぞれが酸化・還元どちらを受けているか答えよ。
鉛蓄電池を一次電池と区別して「二次電池」と呼ぶ理由を答えよ。また二次電池の他の例を2つ挙げよ。
鉛蓄電池で放電を行ったとき、電解液(希硫酸)の密度はどのように変化するか。その理由をH₂SO₄とH₂Oの変化をもとに説明せよ。また、この性質を利用してどのようなことができるか答えよ。
- 【ボルタ電池】負極:Zn→Zn²⁺+2e⁻ 正極:2H⁺+2e⁻→H₂
- 【ダニエル電池】負極:Zn→Zn²⁺+2e⁻ 正極:Cu²⁺+2e⁻→Cu
- 【鉛蓄電池・放電】負極:Pb+SO₄²⁻→PbSO₄+2e⁻ 正極:PbO₂+SO₄²⁻+4H⁺+2e⁻→PbSO₄+2H₂O
- 【鉛蓄電池・放電・全体】Pb+PbO₂+2H₂SO₄→2PbSO₄+2H₂O
- 【鉛蓄電池・充電・全体】2PbSO₄+2H₂O→Pb+PbO₂+2H₂SO₄


コメント