【前回の記事】金属のイオン化傾向 解答・解説
イオン化傾向をまだ確認していない方はこちらから!電池の理解に必要です。
▶ 前回の記事を読む
金属のイオン化傾向を学んだら、次は電池です。電池は「イオン化傾向の差を利用して電気エネルギーを取り出す装置」です。最初に発明された電池「ボルタ電池」の仕組みを理解して、電池の基本原理を身につけましょう!
- 電池の基本原理(イオン化傾向との関係)
- ボルタ電池の構造と各極の反応
- 負極・正極での反応式
- 電子の流れと電流の向き
- 分極とは何か・なぜボルタ電池は長続きしないのか
電池とは、酸化還元反応によって化学エネルギーを電気エネルギーに変換する装置です。
- イオン化傾向の大きい金属が溶け出して電子を放出する(酸化・負極)
- 放出された電子が導線を通って流れる → 電流が生じる
- イオン化傾向の小さい金属側で電子を受け取る反応が起こる(還元・正極)
- 2種類の金属のイオン化傾向の差が大きいほど起電力(電圧)が大きくなる
💡 負極・正極の覚え方
負極(−極)
- イオン化傾向が大きい金属
- 電子を放出する
- 酸化反応が起こる
- 電子が出ていく極
正極(+極)
- イオン化傾向が小さい金属
- 電子を受け取る
- 還元反応が起こる
- 電子が入ってくる極
ボルタ電池は1800年にイタリアの科学者ボルタが発明した、世界最初の電池です。
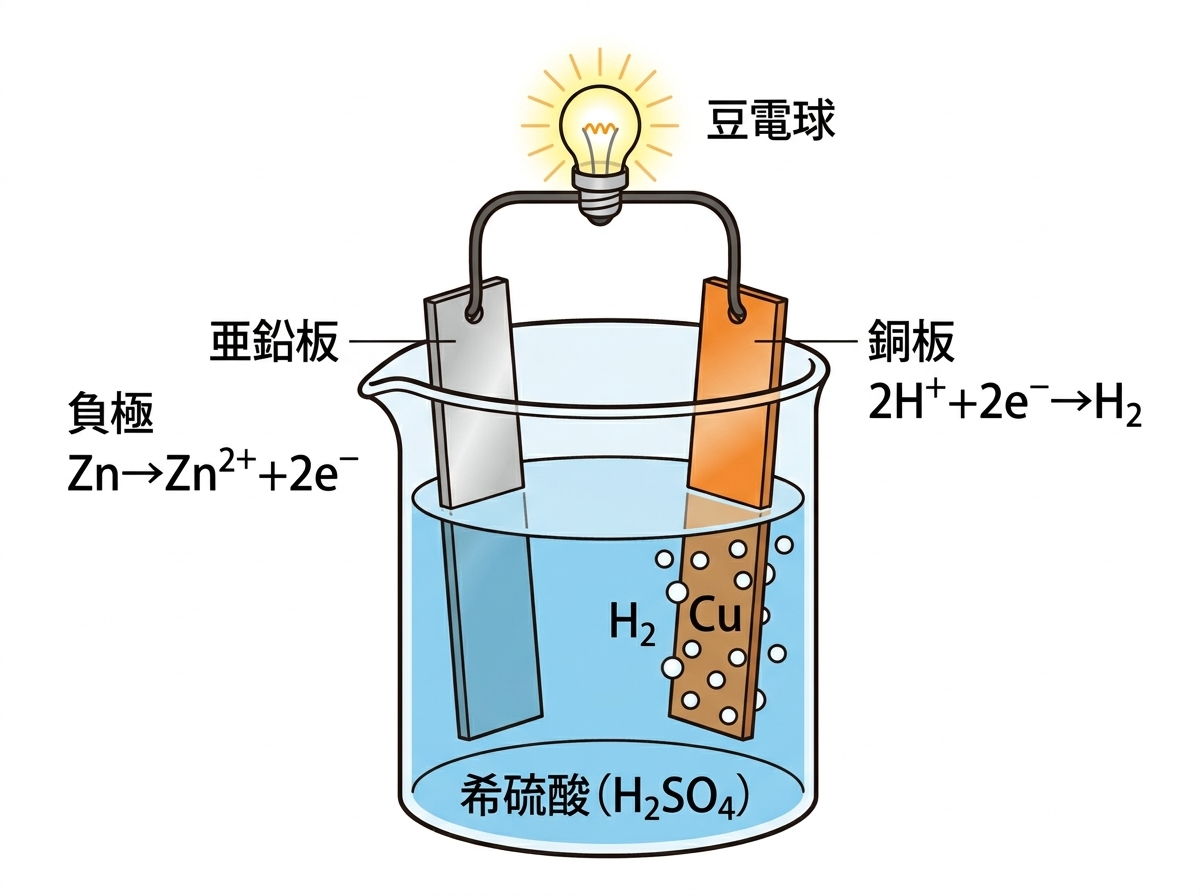
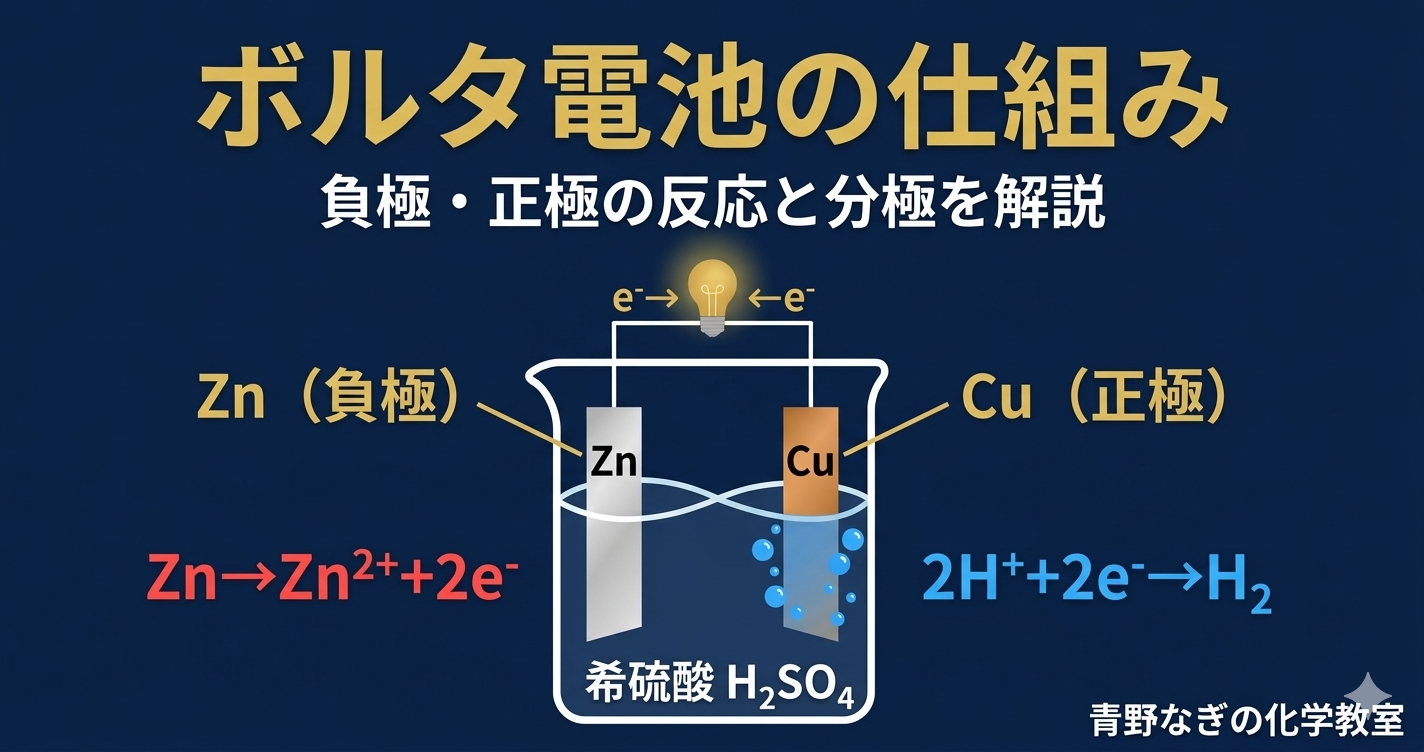
▲ ボルタ電池の構造(亜鉛板:負極、銅板:正極、希硫酸)
Znのイオン化傾向 > Cuのイオン化傾向
Znが溶け出してZn²⁺になる
Zn → Zn²⁺ + 2e⁻
放出されたe⁻が導線を流れる
(希硫酸)
H₂SO₄ → 2H⁺ + SO₄²⁻
導線からe⁻を受け取る
H⁺が還元されH₂が発生
2H⁺ + 2e⁻ → H₂↑
銅板の表面に気泡が発生
ZnがZn²⁺になって電解液に溶け出し、2個のe⁻を放出します。
導線を流れてきたe⁻を、電解液中のH⁺が受け取ってH₂になります。
ZnがH₂SO₄に溶けてZnSO₄になり、H₂が発生する反応です。
| 負極(Zn) | 正極(Cu) | |
|---|---|---|
| 反応の種類 | 酸化 | 還元 |
| 電子の動き | e⁻を放出(出ていく) | e⁻を受け取る(入ってくる) |
| 電子の流れ | Zn極 → 導線 → Cu極 | |
| 電流の向き | Cu極 → 導線 → Zn極(電子と逆向き) | |
電流の向き(+→−)と電子の流れ(−→+)は逆方向です。
電流は「正電荷が流れる方向」と定義されているため、実際に流れる電子とは逆になります。
入試では「電流の向き」と「電子の流れる向き」を区別して答えましょう。
ボルタ電池には大きな欠点があります。それが分極という現象です。
正極(Cu板)でH₂が発生すると、H₂の気泡がCu板の表面に付着します。
H₂の気泡が付着すると…
① H⁺がCu板に到達しにくくなる
② H₂自体がZnに対して正極としてはたらき、逆起電力が生じる
→ 結果として電圧が急激に低下する
分極によってすぐに電圧が下がるため、実用的ではありません。
この欠点を解決したのがダニエル電池です(次の記事で解説)。
- 一次電池:使い切りの電池(ボルタ電池・マンガン乾電池など)
- 二次電池:充電して繰り返し使える電池(鉛蓄電池・リチウムイオン電池など)
- ボルタ電池・ダニエル電池は一次電池
- 電池はイオン化傾向の差を利用して化学エネルギーを電気エネルギーに変換
- 負極:イオン化傾向が大きい金属 → 酸化・e⁻を放出
- 正極:イオン化傾向が小さい金属 → 還元・e⁻を受け取る
- ボルタ電池:負極Zn(Zn→Zn²⁺+2e⁻)・正極Cu(2H⁺+2e⁻→H₂)
- 電子の流れ:Zn→Cu、電流の向き:Cu→Zn(逆向き)
- 分極:Cu板にH₂が付着して電圧が低下する現象 → ボルタ電池の欠点

コメント