【前回の記事】電池の仕組み①ボルタ電池
ボルタ電池の基本原理をまだ確認していない方はこちらから!
▶ 前回の記事を読む
前回学んだボルタ電池には分極という欠点がありましたね。今回はその欠点を解決したダニエル電池を解説します。素焼き板の役割や、なぜ安定した電圧を保てるのかを理解しましょう!
- ダニエル電池の構造と特徴
- 素焼き板(塩橋)の役割
- 負極・正極での反応式
- 電子の流れと電流の向き
- ボルタ電池との違い・なぜ分極が起きないのか
正極(Cu板)でH₂が発生し、Cu板の表面にH₂の気泡が付着することで電圧が急激に低下する現象(分極)が起こります。そのため実用的ではありません。
この欠点を解決するため、1836年にイギリスの科学者ダニエルが考案したのがダニエル電池です。
ダニエル電池の最大の特徴は、2種類の電解質水溶液を素焼き板で仕切っている点です。
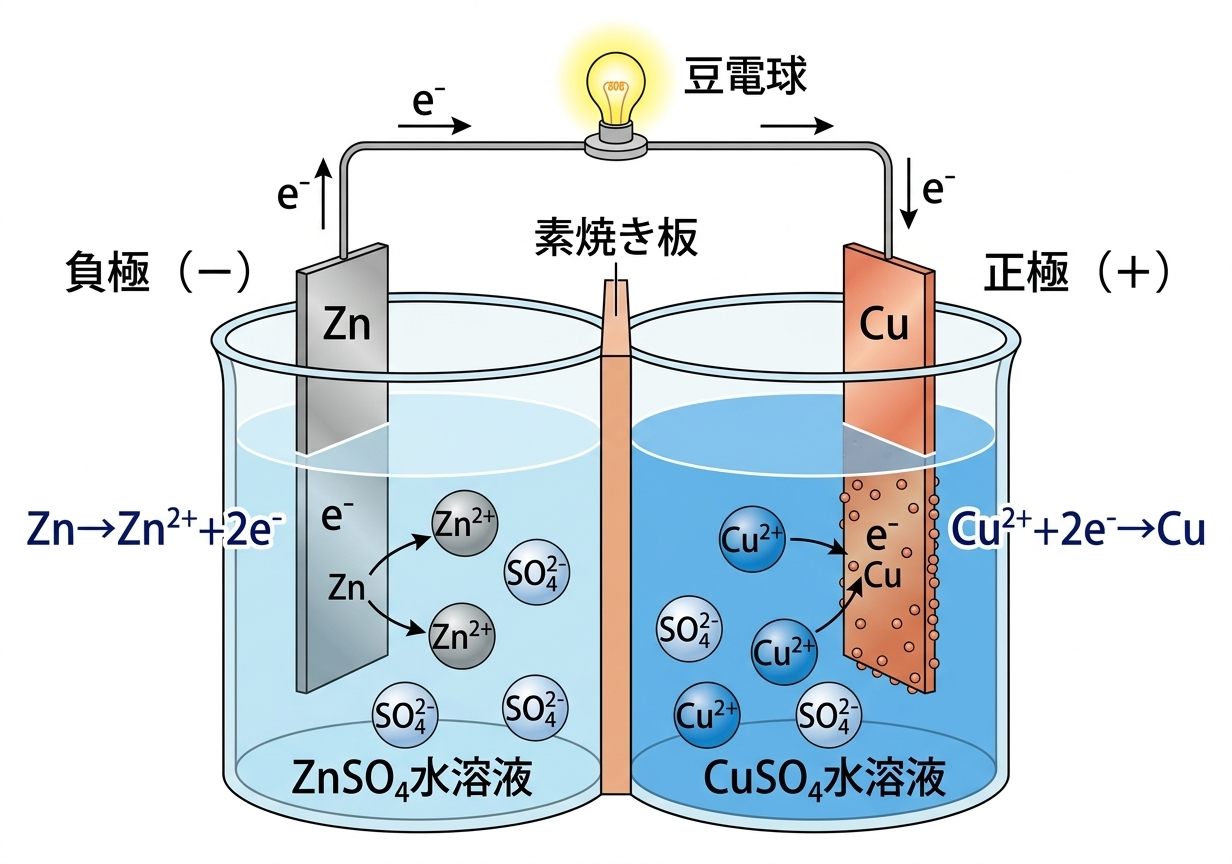
▲ ダニエル電池の構造(左:Zn負極・ZnSO₄、右:Cu正極・CuSO₄、中央:素焼き板)
電解液:ZnSO₄水溶液
Znがイオン化して溶け出す
Zn → Zn²⁺ + 2e⁻
e⁻が導線を通ってCu極へ
(隔膜)
通過
電解液:CuSO₄水溶液
Cu²⁺が電子を受け取りCuが析出
Cu²⁺ + 2e⁻ → Cu
銅板の表面にCuが析出
⚡ 電子・電流の流れ
e⁻の流れ:Zn極 → 導線 → Cu極(負極から正極へ)
電流の向き:Cu極 → 導線 → Zn極(電子と逆向き)
ZnがZn²⁺になってZnSO₄水溶液に溶け出します。
CuSO₄水溶液中のCu²⁺が電子を受け取り、Cu板の表面に析出します。
ZnがCuSO₄に溶けてZnSO₄になり、Cu²⁺が還元されてCuとして析出します。これはイオン化傾向の差による金属の析出(銅樹)と同じ反応です!
ダニエル電池の核心は素焼き板にあります。なぜ素焼き板が必要なのでしょうか?
- 2つの溶液を混ざらないように仕切る(ZnSO₄とCuSO₄を分離)
- イオンだけを通過させる(SO₄²⁻などがゆっくり移動し電気的中性を保つ)
ZnSO₄とCuSO₄が混ざってしまうと、Zn板がCu²⁺と直接反応し導線を通らずに電子が移動してしまいます。これでは電流が生じないため、素焼き板で仕切る必要があります。
負極側ではZn²⁺が増加 → SO₄²⁻が素焼き板を通って移動し電荷を中和
正極側ではCu²⁺が減少 → イオンバランスを保つ
素焼き板のイオン透過によって安定した電圧を維持できます。
- 電極:Zn板・Cu板
- 電解液:希硫酸(1種類)
- 正極の反応:2H⁺ + 2e⁻ → H₂
- 仕切り:なし
- 分極:起こる(H₂が付着)
- 電圧:すぐ低下
- 電極:Zn板・Cu板
- 電解液:ZnSO₄・CuSO₄(2種類)
- 正極の反応:Cu²⁺ + 2e⁻ → Cu
- 仕切り:素焼き板
- 分極:起こらない(H₂が発生しない)
- 電圧:安定して維持
| 負極 | 正極 | 電解液 | 分極 | |
|---|---|---|---|---|
| ボルタ電池 | Zn → Zn²⁺ + 2e⁻ | 2H⁺ + 2e⁻ → H₂ | 希硫酸 | あり |
| ダニエル電池 | Zn → Zn²⁺ + 2e⁻ | Cu²⁺ + 2e⁻ → Cu | ZnSO₄ / CuSO₄ | なし |
| 場所 | 変化 | 理由 |
|---|---|---|
| Zn板(負極) | Zn板が溶けて薄くなる | Znが酸化されZn²⁺として溶け出すため |
| Cu板(正極) | Cu板が厚くなる(Cuが析出) | Cu²⁺が還元されCuとして析出するため |
| CuSO₄水溶液 | 青色が薄くなる | Cu²⁺が消費されるため |
| ZnSO₄水溶液 | Zn²⁺が増加 | Znが溶け出してZn²⁺が増えるため |
- ダニエル電池:負極Zn(ZnSO₄水溶液)、正極Cu(CuSO₄水溶液)を素焼き板で仕切る
- 負極:Zn → Zn²⁺ + 2e⁻(酸化)
- 正極:Cu²⁺ + 2e⁻ → Cu(還元)
- 全体:Zn + CuSO₄ → ZnSO₄ + Cu
- 素焼き板の役割:溶液を仕切り、イオンのみ通過させて電気的中性を保つ
- H₂が発生しないため分極が起こらず、安定した電圧を維持できる

コメント