【前回の記事】電池の仕組み②ダニエル電池
ダニエル電池の仕組みをまだ確認していない方はこちらから!
▶ 前回の記事を読む
ボルタ電池・ダニエル電池は使い切りの一次電池でした。今回学ぶ鉛蓄電池は充電して繰り返し使える二次電池の代表です。自動車のバッテリーにも使われている鉛蓄電池の放電・充電の仕組みを完全理解しましょう!
- 一次電池と二次電池の違い
- 鉛蓄電池の構造(負極・正極・電解液)
- 放電時の各極の反応式
- 充電時の各極の反応式(放電と逆反応)
- 放電・充電で起こる変化(硫酸の濃度変化など)
| 一次電池 | 二次電池 | |
|---|---|---|
| 定義 | 使い切り(充電不可) | 充電して繰り返し使用可能 |
| 例 | ボルタ電池・ダニエル電池・マンガン乾電池 | 鉛蓄電池・リチウムイオン電池・ニッケル水素電池 |
| 充電 | できない | できる(外部電源で逆反応を起こす) |

▲ 鉛蓄電池の実用例:自動車のバッテリー(12V)
鉛蓄電池は1859年にフランスのプランテが発明した二次電池で、現在も自動車のバッテリーとして広く使われています。
材料:鉛(Pb)
放電時:Pbが酸化されPbSO₄に
Pb → PbSO₄
充電時:PbSO₄がPbに戻る
希硫酸
(H₂SO₄)
材料:酸化鉛(PbO₂)
放電時:PbO₂が還元されPbSO₄に
PbO₂ → PbSO₄
充電時:PbSO₄がPbO₂に戻る
- 負極:Pb(鉛)
- 正極:PbO₂(酸化鉛(IV))
- 電解液:希硫酸(H₂SO₄)
- 放電・充電ともに両極にPbSO₄(硫酸鉛)が関与する
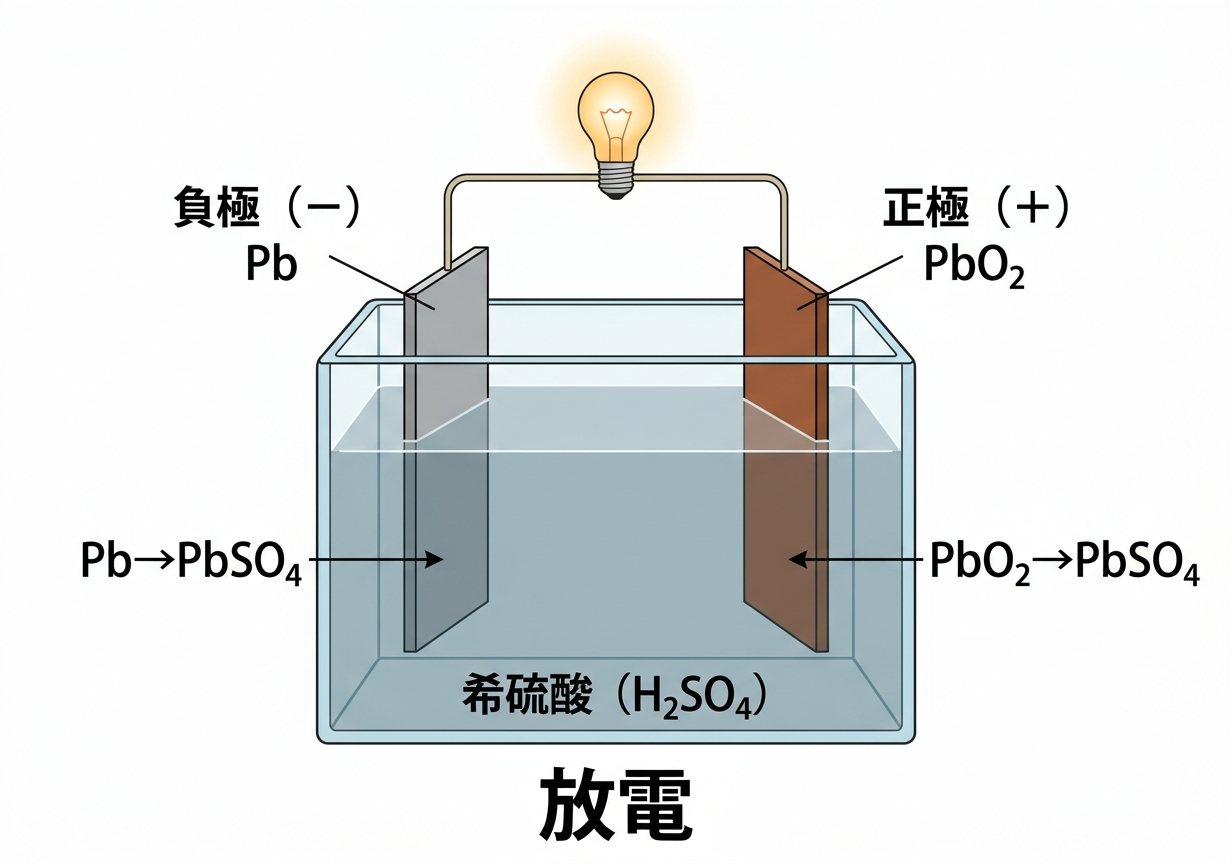
▲ 鉛蓄電池の放電(左:Pb負極、右:PbO₂正極、希硫酸)
PbがSO₄²⁻と反応してPbSO₄になり、2個のe⁻を放出します。
PbO₂がH⁺・SO₄²⁻・e⁻と反応してPbSO₄と水になります。
放電によってH₂SO₄が消費されH₂Oが生成されるため、電解液(希硫酸)の濃度が低下します。
充電とは、外部電源から電気を流して放電の逆反応を起こす操作です。充電時は電極の役割が逆になります。
充電時は外部電源の+極を正極(PbO₂)側、−極を負極(Pb)側につなぎます。
充電時の酸化・還元は放電時と逆になります。
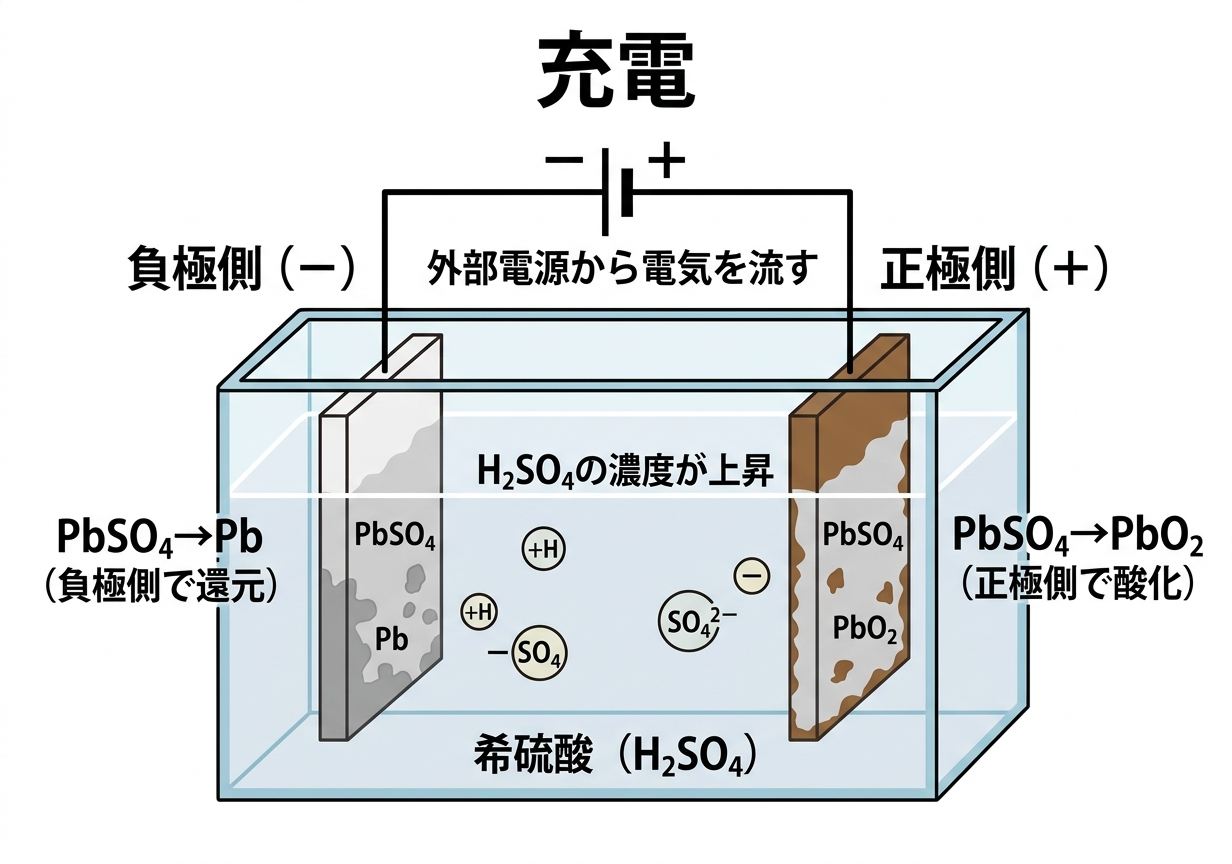
▲ 鉛蓄電池の充電(外部電源から電気を流し放電の逆反応を起こす)
PbSO₄がe⁻を受け取ってPbに戻ります。
PbSO₄がH₂Oと反応してPbO₂に戻ります。
充電によってH₂Oが消費されH₂SO₄が生成されるため、電解液(希硫酸)の濃度が上昇します。
| 放電(電気を使う) | 充電(電気を蓄える) | |
|---|---|---|
| 負極(Pb側) | Pb → PbSO₄(酸化) | PbSO₄ → Pb(還元) |
| 正極(PbO₂側) | PbO₂ → PbSO₄(還元) | PbSO₄ → PbO₂(酸化) |
| H₂SO₄の濃度 | 低下(H₂SO₄消費) | 上昇(H₂SO₄生成) |
| H₂Oの量 | 増加(H₂O生成) | 減少(H₂O消費) |
| PbSO₄ | 両極に生成 | 両極から消費 |
- 電解液の密度を測ることで充電残量を確認できる
- 放電が進む → H₂SO₄が減る → 電解液の密度が低下
- 充電が進む → H₂SO₄が増える → 電解液の密度が上昇
- 自動車バッテリーの点検で「比重計」を使うのはこのため
鉛蓄電池ではPbの酸化数が変化します。入試で酸化数を問われることがあるので確認しましょう。
| 物質 | Pbの酸化数 | 備考 |
|---|---|---|
| Pb | 0 | 単体 |
| PbSO₄ | +2 | SO₄²⁻なのでPb=+2 |
| PbO₂ | +4 | O×2=−4、総和0よりPb=+4 |
負極:Pb(0) → PbSO₄(+2) 酸化数が増加=酸化
正極:PbO₂(+4) → PbSO₄(+2) 酸化数が減少=還元
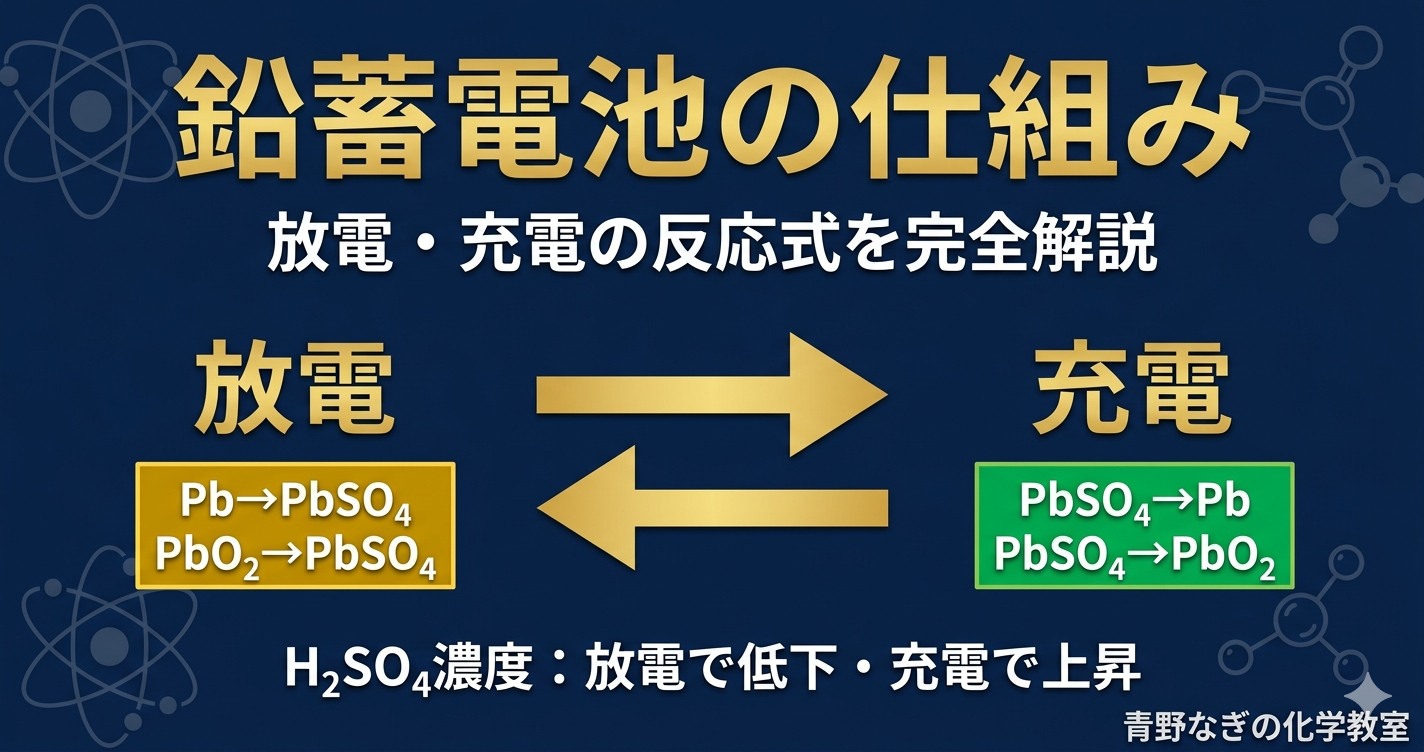
- 鉛蓄電池は二次電池(充電して繰り返し使える)
- 負極:Pb、正極:PbO₂、電解液:希硫酸
- 放電の負極:Pb + SO₄²⁻ → PbSO₄ + 2e⁻
- 放電の正極:PbO₂ + SO₄²⁻ + 4H⁺ + 2e⁻ → PbSO₄ + 2H₂O
- 放電の全体:Pb + PbO₂ + 2H₂SO₄ → 2PbSO₄ + 2H₂O
- 充電は放電の逆反応。放電でH₂SO₄濃度低下、充電で上昇

コメント