【前回の記事】酸化剤・還元剤 練習問題15問 解答・解説
前回の解答・解説をまだ確認していない方はこちらから!
▶ 前回の記事を読む
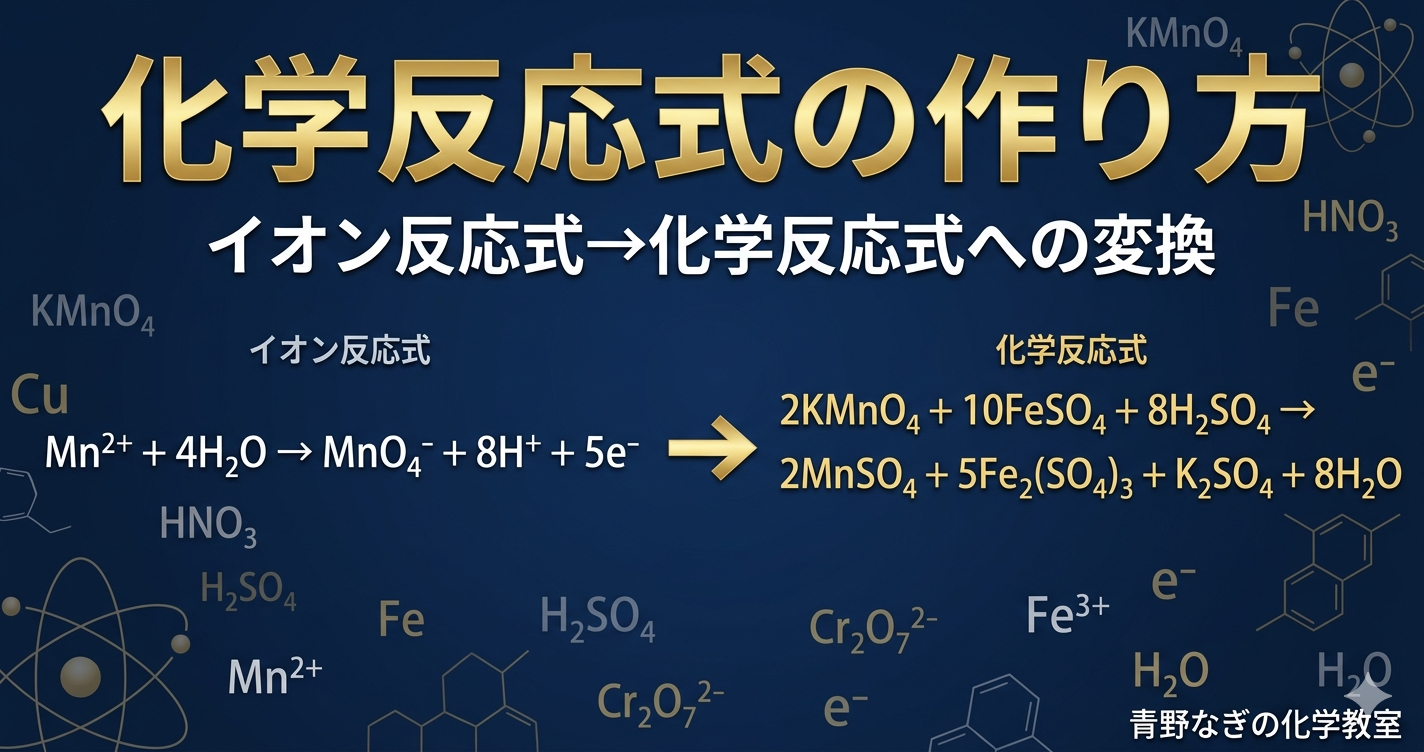
これまで半反応式(イオン反応式)の作り方を学んできました。しかし入試ではイオンを含まない化学反応式を書かせる問題もよく出ます。今回はイオン反応式から化学反応式(分子式)に変換する方法を、具体的な反応例3つを使って丁寧に解説します!
- イオン反応式から化学反応式に変換する手順
- 例題①:硫酸酸性下の過マンガン酸カリウムとシュウ酸の反応
- 例題②:二酸化マンガンと濃塩酸の反応
- 例題③:銅と希硝酸の反応
- 練習問題5題
イオン反応式はイオンのやりとりに注目した式です。これを化学反応式(分子式)に直すには、イオンを元の分子の形に戻す作業が必要です。
- STEP1:酸化剤・還元剤の半反応式を書く
- STEP2:e⁻の数を合わせて足し算し、イオン反応式を作る
- STEP3:イオンを分子の形に戻す(H⁺やOH⁻を対応するイオンと組み合わせる)
- STEP4:両辺を整理して化学反応式の完成
イオン反応式に出てくる主なイオンの戻し方:
・H⁺ + Cl⁻ → HCl(塩酸)
・2H⁺ + SO₄²⁻ → H₂SO₄(硫酸)
・K⁺ + MnO₄⁻ → KMnO₄(過マンガン酸カリウム)
・2K⁺ + SO₄²⁻ → K₂SO₄(硫酸カリウム)
最もよく出る反応の一つです。丁寧に手順を追っていきましょう。
酸化剤(MnO₄⁻)の半反応式:
還元剤((COOH)₂)の半反応式:
(1)×2+(2)×5 でe⁻を10個に合わせる
反応物・生成物のイオンを確認します。
| イオン | 組み合わせるイオン | 分子 | 追加量 |
|---|---|---|---|
| MnO₄⁻ × 2 | K⁺ × 2 | 2KMnO₄ | 両辺にK⁺×2を追加 |
| H⁺ × 6 | SO₄²⁻ × 3 | 3H₂SO₄ | 両辺にSO₄²⁻×3を追加 |
| Mn²⁺ × 2 | SO₄²⁻ × 1(余り) | MnSO₄ × 2 | 右辺のSO₄²⁻×2をMn²⁺と組み合わせる |
| K⁺ × 2(余り) | SO₄²⁻ × 1(余り) | K₂SO₄ | 右辺のK⁺×2とSO₄²⁻×1を組み合わせる |
K:左辺2個、右辺2個 ✅
Mn:左辺2個、右辺2個 ✅
S:左辺3個、右辺3個(2+1) ✅
C:左辺10個(5×2)、右辺10個 ✅
O:左辺 8+10+12=30個、右辺 8+20+8+4=40個…整理して確認を!
MnO₂が酸化剤、HCl(Cl⁻)が還元剤としてはたらきます。
酸化剤(MnO₂)の半反応式:
Mnの酸化数:+4(MnO₂)→ +2(Mn²⁺)(2減少)→ e⁻×2個(左辺へ)
O原子:左辺2個 → 右辺にH₂O×2
H原子:右辺4個 → 左辺にH⁺×4
還元剤(Cl⁻)の半反応式:
Clの酸化数:−1(Cl⁻)→ 0(Cl₂)(1増加)× 2個 = e⁻×2個(右辺へ)
(1)+(2)でe⁻が消える
H⁺×4とCl⁻×2を合わせると HCl が何個できるか考えます。
H⁺×4とCl⁻×4でHCl×4になる
→ Cl⁻が2個足りないので、両辺にCl⁻×2を追加する
→ 左辺:H⁺×4とCl⁻×4 → 4HCl
→ 右辺:Mn²⁺とCl⁻×2 → MnCl₂
HClは4mol使われますが、そのうち酸化還元に関わるのは2mol(Cl⁻×2)のみです。残り2molのHClは酸(H⁺を供給)としてはたらいています。
銅が還元剤、希硝酸が酸化剤としてはたらきます。
酸化剤(HNO₃・希)の半反応式:
還元剤(Cu)の半反応式:
(1)×2+(2)×3 でe⁻を6個に合わせる
左辺:HNO₃×2とH⁺×6 → H⁺は合計8個、NO₃⁻は2個
→ H⁺×6とNO₃⁻×6でHNO₃×6 → さらにHNO₃×2があるので合計8HNO₃
右辺:Cu²⁺×3とNO₃⁻×6 → Cu(NO₃)₂×3
・酸化剤としてはたらくHNO₃:2mol(NO₃⁻がNOになる)
・塩を作るHNO₃:6mol(Cu²⁺と組み合わさりCu(NO₃)₂×3になる)
合計:8mol
- 化学反応式はイオン反応式のイオンを分子の形に戻すことで作れる
- 手順:半反応式 → イオン反応式 → イオンを分子に戻す → 化学反応式
- HClは酸化還元に関わる分と酸としてはたらく分の両方を数える
- HNO₃も酸化剤としての分と塩を作る分の両方を数える
✏️ 練習問題【全5問】
次の反応の化学反応式を作れ。解答・解説は次の記事で確認しましょう!
銅と熱濃硫酸の反応の化学反応式を作れ。
ヒント:酸化剤は熱濃硫酸(H₂SO₄)でSO₂に変化、還元剤はCuでCu²⁺になる
銅と濃硝酸の反応の化学反応式を作れ。
ヒント:酸化剤は濃硝酸(HNO₃)でNO₂に変化、還元剤はCuでCu²⁺になる
銀と希硝酸の反応の化学反応式を作れ。
ヒント:酸化剤は希硝酸(HNO₃)でNOに変化、還元剤はAgでAg⁺になる(Ag → Ag⁺ + e⁻)
硫酸酸性下で過マンガン酸カリウム水溶液にヨウ化カリウム水溶液を加えたときの化学反応式を作れ。
ヒント:酸化剤はMnO₄⁻でMn²⁺に、還元剤はI⁻でI₂になる
硫酸酸性下で二クロム酸カリウム水溶液に過酸化水素を加えたときの化学反応式を作れ。
ヒント:酸化剤はCr₂O₇²⁻でCr³⁺に、還元剤はH₂O₂でO₂になる

コメント